

2023年9月,普米尔医药(Premier Research)助力眼科生物制药公司Ocuphire Pharma和全球医疗保健公司Viatris的产品RYZUMVI™(酚妥拉明滴眼液,0.75%)成功获美国食品药品监督管理局(FDA)批准,用于治疗由肾上腺素能激动剂(如苯肾上腺素)或副交感神经抑制剂(如托吡卡胺)引起的药理学诱导的瞳孔散大。RYZUMVI预计将于2024年上半年在美国上市。

关于RYZUMVI的获批,Viatris眼科健康部门总裁Jeffrey Nau博士表示:“FDA对RYZUMVI的批准,标志着我们眼科健康部门的一个重要里程碑,体现了Viatris致力于推进眼科健康领域发展,并提升眼科健康专业人员和患者的医疗体验的决心。全面的眼科检查,对于视力损害疾病的早期发现至关重要。我们希望通过解决患者的药物性瞳孔散大问题,帮助眼科健康专业人员扩大检查范围,从而提高眼科健康领域的医疗成果。我们期待在明年上半年推出RYZUMVI,并继续推进我们强大的眼科护理产品线,旨在解决一系列视力相关疾病。”
在美国,每年约有1亿人进行全面的眼科检查,其中包括药物引起的瞳孔散大,这种情况可能持续24小时。药物引起的瞳孔散大的副作用包括对光敏感(畏光)和视力模糊,这可能为患者的阅读、工作和驾驶带来影响。

RYZUMVI将有效改善这种现象,而此次普米尔医药在帮助Ocuphire 成功完成505(b)(2) 项目的 PNDA 和 NDA 申报方面发挥了重要作用。普米尔医药通过采用临床桥接和监管策略,利用现有的公共数据降低了药物开发成本,并为RYZUMVI的成功上市大大提速。
普米尔医药在眼科疾病领域具备丰富的专业知识与经验,并设有专业的咨询部门Premier Consulting,可为申办方提供全球临床前至上市后的产品开发全生命周期中的战略及运营解决方案,并深谙美国、欧洲等全球不同地区的监管环境,能够为申办方提供最优监管策略及全方位支持。

截至目前,普米尔医药已为世界各地的申办方完成了3500余种法规事务的成功案例。仅在过去五年中,普米尔医药开展了数量可观的医疗器械研究,涉及心血管、整形外科和联合诊断等众多研究领域。

关于普米尔医药
普米尔医药(Premier Research)目前已经充分掌握肿瘤学和血液学、罕见病、神经科学、全球开发注册策略等各方面领域。依托30多年产品开发经验,公司可以提供从初始策略制定、临床开发再到最终监管申报的一站式全方位服务。如需了解更多信息,欢迎搜索微信公众号”Premier Research”关注垂询。
 女人怀孕后,尽量不要做以下几件事情,对自己和胎儿都不利
女人怀孕后,尽量不要做以下几件事情,对自己和胎儿都不利  生孩子到底有多疼?准爸爸模拟体验“分娩”
生孩子到底有多疼?准爸爸模拟体验“分娩”  宝宝缺铁怎么办 饮食如何改善缺铁情况
宝宝缺铁怎么办 饮食如何改善缺铁情况  阳后别急着造娃,最好推迟两个月再行动
阳后别急着造娃,最好推迟两个月再行动  提醒:科学地“坐月子”才能有助于身体健康的迅速恢复
提醒:科学地“坐月子”才能有助于身体健康的迅速恢复  乙肝妈妈想哺乳,要注意几个细节!
乙肝妈妈想哺乳,要注意几个细节!  孕期这些食物要多吃 推荐这些孕妇健康营养食谱
孕期这些食物要多吃 推荐这些孕妇健康营养食谱  孕妇阳了胎儿会畸形吗?会流产吗?能吃药吗?
孕妇阳了胎儿会畸形吗?会流产吗?能吃药吗?  每天吃一盒蓝莓会发生什么变化 每天吃蓝莓会有什么后果?
每天吃一盒蓝莓会发生什么变化 每天吃蓝莓会有什么后果?  春天养生季,这5种食物可以保护乳房,预防乳腺癌!
春天养生季,这5种食物可以保护乳房,预防乳腺癌!  春季人体生理功能和新陈代谢最活跃的时期,多吃这五大食物
春季人体生理功能和新陈代谢最活跃的时期,多吃这五大食物 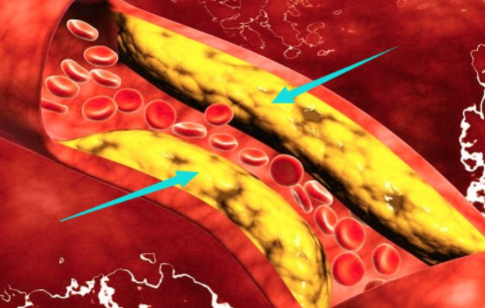 胆固醇高有什么危害 胆固醇高的人不宜吃哪些食物?
胆固醇高有什么危害 胆固醇高的人不宜吃哪些食物?  肾阴虚有什么症状 肾阴虚和肾阳两虚区别
肾阴虚有什么症状 肾阴虚和肾阳两虚区别  立春后依然手脚冰凉?缓解手脚冰冷有哪些小妙招?
立春后依然手脚冰凉?缓解手脚冰冷有哪些小妙招?  网传十大补钙食物你可知道?补钙的食物都有那些?
网传十大补钙食物你可知道?补钙的食物都有那些?  关于家庭常备药连花清瘟的“热知识”与“冷知识”
关于家庭常备药连花清瘟的“热知识”与“冷知识” 