

Paxlovid医保谈判失败-报价过高
2023年1月8日上午8点30分,辉瑞中国区副总裁、市场准入负责人钱飞,进入2023年中国医保谈判会场-北京西城区的全国人大会议中心,于下午13点20分离开现场,耗时四小时50分钟。根据此前披露的信息,本次辉瑞医保谈判涉及包括Paxlovid、特应性皮炎药物、抗感染类药物和抗肿瘤药物在内的7款药物!最终,备受大家关注的辉瑞新冠药物Paxlovid医保谈判以失败告终!根据披露的消息,Paxlovid此次医保谈判价格分歧太大。

全世界范围内P药获批时间线
2021年11月,美国制药巨头辉瑞披露了新冠治疗药物Paxlovid的II/III期EPIC-HR临床试验结果,EPIC-HR研究是一项随机、双盲、安慰剂对照临床试验,旨在研究Paxlovid用于治疗实验室确诊为新冠病毒感染的有症状的非住院成年患者。结果显示,与安慰剂相比,Paxlovid可降低新冠相关住院或死亡风险89%(出现症状后3 d内)和88%(出现症状后5 d内);与安慰剂相比,无非住院、高危成人新冠肺炎患者死亡。在毒副作用方面与安稳剂组没有显著差异。
2021年12月22日,基于上述临床试验结果,FDA紧急批准Paxlovid用于治疗病毒检测呈阳性、有轻度至中度症状,同时病情恶化风险较高的年龄在12岁及以上的患者。
2021年12月26日,欧洲药监局(EMA)紧急批准Paxlovid药物在欧盟成员国中紧急使用。2022年1月,EMA有条件批准Paxlovid用于治疗新冠病毒感染,适应症为用于治疗不需要补氧且有高风险发展为严重治疗感染新冠病毒的成人患者
2022年2月17日,中国国家药监局批准了Paxlovid药物用于新冠肺炎感染患者治疗,Paxlovid的进口审批前后共用时50天,创造了史上最快的新冠药物进口纪录。
目前,Paxlovid在全世界范围内超过40个国家和地区获批。

P药是全球范围内疗效最好的新冠治疗药物
2021年11月4日,英国药品和保健产品监管局(MHRA)批准Molnupiravir(MK-4482,EIDD-2801)上市,用于治疗重症和住院风险较高的轻至中症新冠肺炎(COVID-19)成人患者。FDA于一个月以后紧急批准Molnupiravir用于治疗且有较高风险发展为重症的轻症或中症新冠肺炎(COVID-19)成年患者。Molnupiravir降低住院和死亡的风险比例为50%。
稍后披露的Paxlovid降低住院和死亡的比例为89%。单从这个关键数据来看,Paxlovid疗效显著优于Molnupiravir。
备注:2022年12月底,国际权威医学杂志《柳叶刀》发表临床试验结果:Molnupiravir未降低新冠住院和死亡风险。

国内获批新冠治疗药物
截至2023年1月9日,共有三款新冠治疗药物在国内获批上市:辉瑞Paxlovid(奈玛特韦片/利托那韦片)、河南真实生物阿兹夫定、默沙东公司新冠病毒治疗药物莫诺拉韦胶囊(商品名称:利卓瑞/LAGEVRIO)。
在前文中我们介绍了Paxlovid和Molnupiravir的临床试验结果,作为国内唯一一款获批的阿兹夫定临床效果到底如何?
阿兹夫定的临床试验结果尚未正式发表,根据预印本发表的结果显示:阿兹夫定可显著缩短轻、中度SARS-CoV-2感染患者的核酸转阴时间、加快病毒消除、显著降低病毒载量、减轻患者症状、缩短病程, 且安全性良好、对患者肝肾功能无显著影响,安全有效。
国内在研新冠治疗药物
目前国内有6款药物进入临床III期试验研究阶段,包括:先声药业SIM0417、君实生物VV116、众生药业RAY1216、前沿生物FB2001、广生堂GST-HG171、开拓药业普克鲁胺。
先声药业SIM0417有望最快获批!2022年12月26日,江苏省药监局发文披露,先声药业SIM0417已经完成III期临床试验入组,预计最快2023年2月份上市。
君实生物VV116是目前国内在研新冠药物中唯一披露临床试验结果的药物。2022年12月29日,全球权威学术期刊《新英格兰医学》杂志(The New England Journal of Medicine,NEJM,影响因子:176.079),披露了VV116治疗新冠肺炎的III期临床试验结果。结果显示:研究主要终点达到设计的非劣效终点,相比PAXLOVID,VV116组的临床恢复时间更短,安全性方面的顾虑更少。

国产新冠治疗药物与Paxlovid相比疗效如何?
Paxlovid已经做了三个三期临床试验,目前的结果是:一个成功,两个失败:辉瑞Paxlovid之所以快速获得FDA、EMA等机构的批准主要是基于其II/III期EPIC-HR临床试验结果,能够显著降低住院和死亡的比例达到89%。此外,2022年,Paxlovid另外两个III期临床试验宣告失败!2022年4月29日,辉瑞宣布Paxlovid用于暴露后预防的II/III期临床(EPIC-PEP)结果,未达到降低通过家庭接触暴露于新冠病毒的成人感染(确诊)风险的主要研究终点。2022年6月15日,辉瑞公布了新冠口服药Paxlovid针对未接种疫苗的成年人以及具有一种或多种进展为重症疾病风险因素的已接种疫苗成年人的II/III期临床(EPIC-SR)研究结果,未达到所有症状连续4天持续缓解的主要终点,次要终点不具有统计学意义。
君实生物VV116与Paxlovid头对头非劣:君实生物在Clinical Trial注册做个临床试验,其中最重要的一个即为与Paxlovid头对头的试验。一开始,这个III期临床试验主要是想看看与Paxlovid相比,降低住院和死亡的疗效 到底如何?但在后续临床试验开展的过程中,删掉了这个大家最为关注的终点(根据Clinical trial数据库显示,临床试验方案前后修改3次,有一种说法是当时入组的患者重症太少,不得已修改临床终点!)。

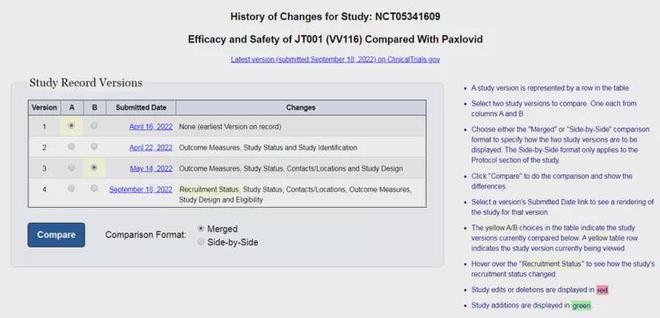
纵观国内已经获批或者有临床试验披露的国产新冠治疗药物,无论是阿兹夫定还是VV116,在大家最为关注的降低重症和死亡方面没有任何可分析的数据披露。而有人说VV116跟Paxlovid相比,不是非劣么? VV116对标Paxlovid的临床终点虽然是非劣,问题是Paxlovid自己做的相关的III期临床试验都已经失败了。不客气地讲,你去对标一个已经临床失败的III期临床试验。这也是为什么虽然VV116的III期临床试验9月份已经结束,却迟迟没有看到其获批的消息。数据库查询可以看到,VV116在2022年12月15日,注册了一个新的III期临床试验。
医保谈判的“以量换价”逻辑,对当下的辉瑞Paxlovid没有吸引力
前几年,医保谈判“灵魂砍价”走红互联网,为大家津津乐道,甚至心里还有一种“痛快”的错觉!但凡参与医保谈判成功的药物,无一例外都有大幅度地降价!而对于辉瑞来讲,Paxlovid铁定超过阿达木单抗,成为“药王”!在2022年Q1销售额达到14.7亿美元,Q2销售额快速增长到了81亿美元,Q3季度销售额75亿美金,前三季度销售额达到了惊人的170亿美金。预计年最高销售额度超过300亿美金。目前在新冠治疗领域,全球范围内没有哪一个药物能够在临床试验中击败Paxlovid,换句话说辉瑞拥有全球市场的绝对优势。
而反观国内,我们不得不承认的一个尴尬事实:目前已经上市或者在研的药物,同样是没有任何一个药物能够在降低重症和死亡方面击败辉瑞Paxlovid!在现阶段新冠感染重症或者非重症的临床治疗中Paxlovid仍然是医生的首选药物!
对于患者来讲,好的消息是:根据第十版的新冠治疗指南,辉瑞Paxlovid目前还在医保支付的范围,截止日期到2023年3月31日。
我们期待国内的药物研发企业尽快能够拿出令人信服的临床试验数据。到那个时候,谁又会在乎Paxlovid能不能进医保呢?
 提醒:科学地“坐月子”才能有助于身体健康的迅速恢复
提醒:科学地“坐月子”才能有助于身体健康的迅速恢复  乙肝妈妈想哺乳,要注意几个细节!
乙肝妈妈想哺乳,要注意几个细节!  孕期这些食物要多吃 推荐这些孕妇健康营养食谱
孕期这些食物要多吃 推荐这些孕妇健康营养食谱  孕妇阳了胎儿会畸形吗?会流产吗?能吃药吗?
孕妇阳了胎儿会畸形吗?会流产吗?能吃药吗?  乳腺癌容易盯上哪些人?
乳腺癌容易盯上哪些人?  白带发黄是宫颈癌的警示吗?
白带发黄是宫颈癌的警示吗?  超高龄生育,这几件事你准备好了吗?
超高龄生育,这几件事你准备好了吗?  孩子发烧、恶心、呕吐!竟然是心理出了问题
孩子发烧、恶心、呕吐!竟然是心理出了问题  试试4条“黄金”法则 或能让你睡个好觉
试试4条“黄金”法则 或能让你睡个好觉  泡氡温泉对身体有害还是有益?
泡氡温泉对身体有害还是有益?  男人肾虚三个危害,个个都是要命的手!
男人肾虚三个危害,个个都是要命的手!  女性更年期如何保持健康与美丽?
女性更年期如何保持健康与美丽?  坚持早睡身体会有什么变化?
坚持早睡身体会有什么变化?  抑郁的人,这4类食物尽量少碰,或助改善情绪
抑郁的人,这4类食物尽量少碰,或助改善情绪  多吃3样粗粮,健脾胃,营养滋补暖身
多吃3样粗粮,健脾胃,营养滋补暖身  南京一男子每天1包烟4年2次心梗
南京一男子每天1包烟4年2次心梗